印染废水水量大,污染物成分复杂[1],是工业废水主要来源之一.生物处理法运行简单且价格低廉,是印染废水的传统处理方法[2-3],但由于该废水是“高毒性”和“难降解”两大主要特性的叠加,因此难以保证稳定的处理效果.近年来,国家对纺织染整工业水污染物的排放标准日益严格,现有的生物处理工艺很难达到要求.目前,有应用前景的印染废水处理工程化技术主要有氧化法[4-5]和吸附法[6].吸附法成本较氧化法稍低,但传统的活性炭、泥炭和壳聚糖等对染料的吸附容量较低,并且需要考虑吸附剂的再生问题,因此研发稳定、利用率高且集吸附与转化于一体的新型环境功能材料是强化吸附处理技术的必然趋势.20世纪90年代以后,随着现代分析技术和测试手段的广泛应用,人们发现层状双金属氢氧化物 (LDHs)[7]具有金属离子、结晶水、层间阴离子、层板与层析的排列顺序等微观结构和层板电性及较大的比表面积,逐渐成为环境功能材料的研究热点.在水处理应用中,层状双金属氢氧化物主要作为吸附剂,以去除水中的重金属离子、无机阴离子和染料等[8-11].随着研究的深入,可以通过掺杂一些具有催化活性的金属离子和石墨烯等以增加LDHs的高级氧化作用,提高污染物的降解并实现吸附剂的原位活化再生[12].
本文以MgAl-LDHs为前驱体,采用共沉淀法将EDTACo嵌入到LDHs中,成功合成了新型纳米多功能复合材料,通过X射线衍射仪 (XRD)、电感耦合等离子体发射光谱仪 (ICP) 和比表面积 (BET) 分析技术对该材料的晶体结构、组成和表面积进行表征,并以偶氮染料活性黑5为目标污染物,研究了废水浓度、pH、温度等因素对吸附效果的影响,初步探讨了其作为类Fenton催化剂的反应性能.
1 实验部分 1.1 实验试剂与材料主要试剂:氯化镁、氯化铝、硝酸镁、硝酸铝、碳酸钠、氢氧化钠、EDTA二钠、氯化钴、活性黑5均为分析纯,购自国药化学集团.
1.2 吸附剂制备方法[11, 13]将一定质量的Na2CO3和NaOH混合溶解于高纯水中,置于自滴液漏斗中,备用.将按一定比例配制的MgCl2·6H2O和AlCl3·6H2O混合溶解于高纯水,并置于500 mL的四颈蒸馏瓶,然后将其放到自控调温装置的油浴中,采用电动搅拌器进行搅拌.当温度达到40 ℃时,将Na2CO3和NaOH混合液逐滴滴加到蒸馏瓶中进行反应.滴加完毕后,将油浴温度升至100 ℃晶化16 h.样品冷却后,将沉淀产物进行抽滤,用高纯水多次洗涤至中性及无游离的氯离子,再用丙酮洗涤二次,在80 ℃下烘干、研磨,备用.
称取一定质量的EDTANa2和CoCl2·6H2O分别溶于高纯水,然后将EDTA-2Na溶液加入到置于油浴中的三颈蒸馏瓶.当温度升至70 ℃时,用连续滴加器将CoCl2·6H2O滴加到蒸馏瓶中发生络合反应,滴加完成后,并持续恒温反应30 min,得到[EDTACo]Na2溶液.
称取一定质量的MgAl-LDHs并加入高纯水,然后转移到250 mL的三颈蒸馏烧瓶,最后将其置于100 ℃的油浴中.当油浴温度升至100 ℃时,将制得的[EDTACo]Na2溶液通过自动加液器逐滴滴加至三颈瓶中,并使其在100 ℃的油浴中晶化老化16 h.冷却后,将反应产物进行抽滤,用高纯水多次洗涤至中性及无游离离子,再用丙酮洗涤二次,在80 ℃下烘干、研磨,备用.
1.3 实验方法 1.3.1 吸附性能采用控制变量法:在若干个100 mL的磨口玻璃瓶内,称取一定质量的吸附剂并加入待测溶液,在恒温振荡器中进行吸附,测定不同条件下吸附质浓度.
1.3.2 吸附等温线采用批量平衡振荡法:在若干个100 mL磨口锥形瓶内,称取一定质量的吸附剂并加入到含有一系列不同浓度吸附质的溶液,在恒温振荡器中进行吸附,直到达到吸附平衡.用0.5 μm玻璃纤维滤膜过滤,然后确定溶液中剩余吸附质的浓度.吸附量的计算方法如下所示:
| $ {q_{\rm{e}}} = \frac{{({\rho _0}{\rho _{\rm{e}}})V}}{m} $ | (1) |
式中:qe是平衡吸附量,mg·g-1;ρ0是初始吸附质质量浓度,mg·L-1;ρe是吸附平衡后,剩余吸附质质量浓度,mg·L-1;V是溶液体积,L;m是吸附剂投加量,g.
在Langmuir等温吸附模型中,通常利用Langmuir系数KL计算分离常数RL,以此来表征吸附反应进行的难易程度,如下所示:
| $ {R_{\rm{L}}} = \frac{1}{{1 + {K_{\rm{L}}}{\rho _0}}} $ | (2) |
在若干个100 mL磨口锥形瓶内,称取0.4 g·L-1的吸附剂并加入含有不同浓度吸附质的溶液 (未调节溶液pH值,约为6.5),在恒温振荡器中进行吸附.反应2 h后,加入0.8 mmol的H2O2,反应1 h,然后确定溶液中剩余吸附质的浓度.
1.4 分析、表征方法活性黑5浓度的测定,采用紫外分光光度法,最大吸收波长为599 nm.
采用德国布鲁克公司D08型X射线衍射仪表征样品的晶体结构,Cu靶,电流为80 mA,电压为40 kV,扫描范围为3°~80°,扫描速度为0.02(°)·min-1.
将LDHs样品用1:1(体积比) 的盐酸溶解后,再用去离子水稀释,最后用Optima 2100 DV电感耦合等离子体发射光谱仪测定.通过金属元素的含量得出二价和三价金属的比例以及层板金属元素比例的变化.
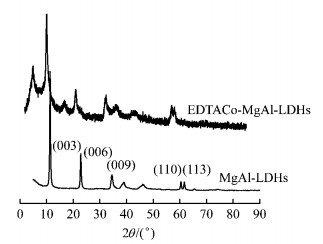
2 结果与讨论 2.1 EDTACo-MgAl-LDHs表征对照MgAl-LDHs的特征衍射峰可知,在相近的角度范围内,EDTACo-MgAl-LDHs出现MgAl-LDHs的 (003)、(006)、(009) 和 (110)、(113) 特征峰 (见图 1).d003、d006、d009之间存在良好的倍数关系,且峰形尖锐、基线平衡、杂峰少,谱峰对称性好,基线及其峰形与MgAl-LDHs相近,表明嵌入EDTACo后的EDTACo-MgAl-LDHs具有规整的层状结构,晶相单一, 结构合理、完整,没有因为EDTACo的嵌入而改变LDHs的结构.
|
图 1 MgAlLDHs和EDTACoMgAlLDHs的XRD图谱 Fig.1 XRD patterns of MgAl-LDHs and EDTACo-MgAl-LDHs |
电感耦合等离子体光谱分析结果表明,EDTACo-MgAl-LDHs层间金属离子Mg和Al的物质的量比约为3:1,与MgAl-LDHs材料相似.由于EDTACo络合离子的嵌入,C、N元素从MgAl-LDHs中含量5.43%和0分别提高到13.00%和3.50%左右.
比表面积分析结果表明,MgAl-LDHs的比表面积为125 m2·g-1,EDTACo-MgAl-LDHs为189 m2·g-1,较MgAl-LDHs比表面积提高了近50%,表明该制备方法提高了前驱体材料的空隙率,有利于其作为吸附剂的应用.
2.2 吸附性能分析25 ℃、pH为6.5条件下, 0.8 g·L-1吸附剂对活性黑5的吸附效果如图 2所示.由图可知,吸附量随吸附质质量浓度的增大而增加.在高初始浓度时,吸附量随着时间的延长明显经历两个阶段,开始的60 min内吸附量快速增长,而后的120 min内,吸附量随着时间的延长平缓增长,180 min后趋于平稳,400 mg·L-1的吸附质浓度所能达到的饱和吸附量为330 mg·g-1左右.同样条件下,相较于MgAl-LDHs的最大平衡吸附量68.43 mg·g-1,EDTACo-MgAl-LDHs的吸附量增大了3.8倍以上.

|
图 2 EDTACoMgAlLDHs对活性黑5的吸附量随时间的变化 Fig.2 Adsorption capacity of reactive black 5 by EDTACo-MgAl-LDHs with varied time |
目前用于水溶液中活性黑5的吸附剂类型主要有泥炭、活性炭等.泥炭和城市飞灰[14]的吸附能力非常弱,吸附量均小于10 mg·g-1,不宜用作活性黑5的吸附剂;活性炭和商用活性炭颗粒F400两类吸附剂[15]的吸附量分别为58.82 mg·g-1和176 mg·g-1, 碱性法和十二烷基硫酸钠法制得的壳聚糖[16]对活性黑5的吸附量分别为201.9 mg·g-1和168.07 mg·g-1;由虾壳制备的壳聚糖粉和壳聚糖膜[17]对活性黑5的吸附量分别为196.9 mg·g-1和194.7 mg·g-1.对比各吸附剂的吸附量可得,本文制备的EDTACo-MgAl-LDHs吸附剂对活性黑5的吸附量大大高于商业活性炭颗粒,且优于多数已知的吸附剂.相较于MgAl-LDHs[18]和MgNiAl-LDH[19]对甲基橙染料的平衡吸附量148 mg·g-1和375 mg·g-1(后者吸附量是前者的2.5倍),EDTACo-MgAl-LDHs可以广泛应用于类似偶氮染料如活性黑5、甲基橙等的印染废水中.
2.3 初始pH的影响pH在LDHs吸附去除有机阴离子污染物的过程中有着重要影响.一方面, pH变化会引起材料组成发生变化;另一方面,pH的大小决定了阴离子有机污染物在水中的存在形态以及水体的性质.25 ℃、0.8 g·L-1 EDTACo-MgAl-LDHs对400 mg·L-1活性黑5吸附3 h的效果随溶液初始pH的变化如图 3所示.

|
图 3 初始pH对EDTACoMgAlLDHs吸附活性黑5去除率的影响 Fig.3 Effect of initial pH on removal ratio of reactive black 5 by EDTACo-MgAl-LDHs |
由图 3可知,EDTACo-MgAl-LDHs对活性黑5的去除率随着pH的升高呈先增大后减小的趋势.当pH值介于4~10之间时,其吸附去除率均介于65%~70%之间; 当pH值为2和12时,吸附剂EDTACo-MgAl-LDHs的吸附效果较差.这是因为:当pH较小时,LDHs层板发生部分溶解,导致结构破坏;当pH较高时,水体中存在的OH-浓度增大,形成对有机物吸附的竞争,大大降低污染物去除率[20].
2.4 温度的影响吸附过程中能量的变化和温度有着密切的关系,吸附剂在不同温度下往往有着不同的吸附状况,探讨温度因素的影响有着重要意义.
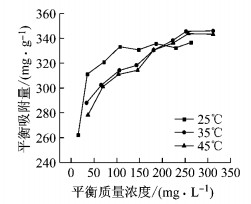
在pH为6.5条件下,0.8 g·L-1 EDTACo-MgAl-LDHs对400 mg·L-1活性黑5在25、35、45 ℃温度下的吸附量如图 4所示.从图中可以看出,在相对应的平衡浓度下,温度对于EDTACo-MgAl-LDHs在低浓度和高浓度范围内的吸附具有不同的影响规律.这是因为:EDTACo-MgAl-LDHs对于溶液中活性黑5的吸附以化学吸附为主,当吸附质浓度较低时,溶液和吸附剂表面聚集的离子基团较少,温度成为吸附的主要因素,又由于活性黑5的吸附过程是放热反应,温度升高,吸附量减小;当吸附质浓度较高时,溶液和吸附剂表面聚集了大量的离子基团,吸附剂表层及其空隙的电子、离子基团相互作用的影响远远大于由于温度的升高对吸附量的影响.
|
图 4 不同温度下EDTACoMgAlLDHs的吸附量 Fig.4 Adsorption capacity of EDTACo-MgAl-LDHs for reactive black 5 at different temperatures |
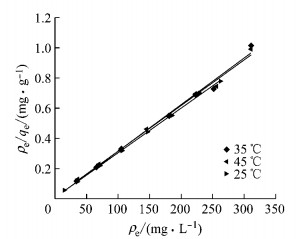
EDTACo-MgAl-LDHs的吸附数据与Langmuir等温吸附模型具有很强的相关性,其在25、35、45 ℃的相关性系数R2分别为:0.999、0.988和0.992,且其理论吸附量与实验吸附量很接近,这说明Langmuir吸附等温方程适合描述EDTACo-MgAl-LDHs对溶液中活性黑5的等温吸附过程.在Langmui等温吸附模型中,通常利用Langmuir系数KL可以计算出分离常数RL,以此来表征吸附反应进行的难易程度 (见式 (2)).当RL>1时,表示吸附难于进行;当RL=1时,表示等温吸附为线性;当0 < RL < 1时,表示吸附过程容易进行.从图 5可以看出,拟合的线性方程截距大于零,说明KL大于零,所以0 < RL < 1且随着初始浓度增大而增大,RL减小直至基本恒定,其吸附的难易程度不再变化.当初始质量浓度大于200 mg·L-1,EDTACo-MgAl-LDHs吸附的RL为0.02,不会因为初始浓度的增加而使得吸附更易于发生.
|
图 5 EDTACoMgAlLDHs吸附溶液中活性黑5的Langmuir吸附等温线 Fig.5 Langmuir plots of the adsorbent EDTACo-MgAl-LDHs for reactive black 5 adsorption |
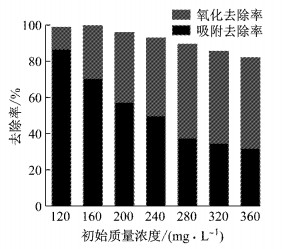
为了考察EDTACo-MgAl-LDHs作为吸附剂和催化剂的双重效果,降低EDTACo-MgAl-LDHs的投加量至0.4 g·L-1,且将吸附时间缩短至2 h,在吸附未饱和的情况下加入0.8 mmol H2O2继续反应1 h,检测剩余活性黑5的浓度,如图 6所示.
|
图 6 EDTACoMgAlLDHs对不同初始质量浓度活性黑5的吸附和催化氧化性能 Fig.6 Adsorption and catalytical oxidation of EDTACo-MgAl-LDHs for reactive black 5 with different initial concentrations |
由图 6可知,随着初始浓度的增大,其吸附去除效率逐渐减小,由85%降低到35%左右,而EDTACo-MgAl-LDHs的氧化去除效率随着初始质量浓度的增加而增大.对于初始浓度在120~360 mg·L-1的活性黑5,其总去除率可达90%以上.因此,EDTACo-MgAl-LDHs不仅能够有效地吸附活性黑5,还能通过催化H2O2进一步氧化去除残留的活性黑5,在有毒、难降解有机污染物的去除中具有非常好的应用潜力.
3 结论(1) EDTACo-MgAl-LDHs结晶度好,晶相单一,结构合理、完整,具有规整的层状结构,是理想的层状双金属结构.EDTACo-MgAl-LDHs的比表面积为189 m2·g-1,较MgAl-LDHs提高了近50%.
(2) EDTACo-MgAl-LDHs吸附溶液中活性黑5的pH适用范围较广,其数值介于4~10之间均具有较好的吸附效果.
(3) 温度对EDTACo-MgAl-LDHs吸附活性黑5的效果影响不大,常温、中性pH条件下EDTACo-MgAl-LDHs对活性黑5的饱和吸附量为330 mg·g-1左右,较MgAl-LDHs的最大平衡吸附量提高了3.8倍以上,大大高于商业活性炭颗粒,且优于多数已知的吸附剂.
(4) 随着污染物浓度的增大,EDTACo-MgAl-LDHs的吸附和氧化效果呈互补趋势,对于初始质量浓度在120~360 mg·L-1范围内活性黑5的总去除率均能达到90%以上.
| [1] |
PEARCE C I, LLOYD J R, GUTHRIE J T. The removal of colour from textile wastewater using whole bacterial cells: a review[J]. Dyes and Pigments, 2003, 58(3): 179 DOI:10.1016/S0143-7208(03)00064-0 |
| [2] |
YILMAZ A, YILMAZ E, YILMAZ M, et al. Removal of azo dyes from aqueous solutions using calix[J]. Dyes and Pigments, 2007, 74(1): 54 DOI:10.1016/j.dyepig.2006.01.011 |
| [3] |
KALYUZHNYI S, YEMASHOVA N, FEDOROVICH V. Kinetics of anaerobic biodecolourisation of azo dyes[J]. Water Science & Technology, 2006, 54(2): 73 |
| [4] |
WANG C, YEDILER A, LIENERT D, et al. Ozonation of an azo dye CI Remazol Black 5 and toxicological assessment of its oxidation products[J]. Chemosphere, 2003, 52(7): 1225 DOI:10.1016/S0045-6535(03)00331-X |
| [5] |
HE J, MA W, HE J, et al. Photo oxidation of azo dye in aqueous dispersions of H2O2/α-FeOOH[J]. Applied Catalysis B: Environmental, 2002, 39(3): 211 DOI:10.1016/S0926-3373(02)00085-1 |
| [6] |
GUPTA V K, SUHAS. Application of low-cost adsorbents for dye removal: a review[J]. Journal of Environmental Management, 2009, 90(8): 2313 DOI:10.1016/j.jenvman.2008.11.017 |
| [7] |
THEISS F L, AYOKO G A, FROST R L. Synthesis of layered double hydroxides containing Mg2+, Zn2+, Ca2+ and Al3+ layer cations by co-precipitation methods: a review[J]. Applied Surface Science, 2016, 383(33): 200 |
| [8] |
LIANG X F, ZANG Y B, XU Y M, et al. Sorption of metal cations on layered double hydroxidesdes[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2013, 433(35): 122 |
| [9] |
ASHEKUZZAMAN S M, JIANG J Q, et al. Study on the sorption-desorption-regeneration performance of Ca-, Mg-and CaMg-based layered double hydroxides for removing phosphate from water[J]. Chemical Engineering Journal, 2014, 246(12): 7 |
| [10] |
LING F L, FANG L, LU Y, et al. A novel CoFe layered double hydroxides adsorbent: high adsorption amount for methyl orange dye and fast removal of Cr (Ⅵ)[J]. Microporous and Mesoporous Materials, 2016, 234: 230 DOI:10.1016/j.micromeso.2016.07.015 |
| [11] |
GUZMÁN-VARGASA A, LIMA E, URIOSTEGUI-ORTEGA GISSELLE A, et al. Adsorption and subsequent partial photodegradationof methyl violet 2B on Cu/Al layered double hydroxides[J]. Applied Surface Science, 2016, 363: 372 DOI:10.1016/j.apsusc.2015.12.050 |
| [12] |
DAUD M, KAMAL M S, SHEHZAD F, et al. Graphene/layered double hydroxides nanocomposites: a review of recent progress in synthesis and applications[J]. Carbon, 2016, 104: 241 DOI:10.1016/j.carbon.2016.03.057 |
| [13] |
HOSNI K, SRASRA E. Evaluation of phosphate removal from water by calcined-LDH synthesized from the dolomite[J]. Colloid Journal, 2010, 72(3): 423 DOI:10.1134/S1061933X10030178 |
| [14] |
JAIN A K, GUPTA V K, BHATNAGAR A, et al. Utilization of industrial waste products as adsorbents for the removal of dyes[J]. Journal of Hazardous Materials, 2003, 101(1): 31 DOI:10.1016/S0304-3894(03)00146-8 |
| [15] |
MCKAY G, IP A W M, BARFORD J P. Reactive black dye adsorption/desorption onto different adsorbents: effect of salt, surface chemistry, pore size and surface area[J]. Journal of Colloid and Interface Science, 2009, 337(1): 32 DOI:10.1016/j.jcis.2009.05.015 |
| [16] |
WOO S H, CHATTERJEE S, CHATTERJEE T. Influence of the polyethyleneimine grafting on the adsorption capacity of chitosan beads for Reactive Black 5 from aqueous solutions[J]. Chemical Engineering Journal, 2011, 166(1): 168 DOI:10.1016/j.cej.2010.10.047 |
| [17] |
DOTTO G L, OCAMPO-PEREZ R, MOURA J M, et al. Adsorption rate of Reactive Black 5 on chitosan based materials: geometry and swelling effects[J]. Adsorption, 2016, 22: 973 DOI:10.1007/s10450-016-9804-y |
| [18] |
AI L H, ZHANG C Y, MENG L Y. Adsorption of methyl orange from aqueous solution on hydrothermal synthesized Mg-Al layered double hydroxide[J]. Journal of Chemical & Engineering Data, 2011, 56(11): 4217 |
| [19] |
ZAGHOUANE-BOUDIAF H, BOUTAHALA M, ARAB L. Removal of methyl orange from aqueous solution by uncalcined and calcined MgNiAl layered double hydroxides (LDHs)[J]. Chemical Engineering Journal, 2012, 187: 142 DOI:10.1016/j.cej.2012.01.112 |
| [20] |
周友飞, 隋铭皓, 盛力. 层状双金属氢氧化物在有机污染物吸附方面的应用[J]. 水处理技术, 2012, 38(11): 1 ZHOU Youfei, SUI Minghao, SHENG Li. Application of layered double hydroxides in adsorption on organic pollutants[J]. Technology of Water Treatment, 2012, 38(11): 1 DOI:10.3969/j.issn.1000-3770.2012.11.001 |
 2017, Vol. 45
2017, Vol. 45
