随着石油资源的过度消耗和环境保护问题的日渐突出,世界各国都在寻找发动机清洁环保的替代燃料.乙醇(C2H5OH)作为一种辛烷值高、含氧且燃烧热效率高的可再生燃料,与汽油掺混燃用已得到学术界和工程领域的广泛关注.目前我国使用的乙醇汽油均为无水乙醇汽油.无水乙醇制备工艺复杂、成本较高.若在乙醇制备过程中省去最后的脱水精制工艺,只得到纯度约为95%的含水乙醇,则可大大降低生产的能耗和成本.因此,汽车行业大力推广使用的含水乙醇汽油具有极高的经济效益[1].
汽油是由150多种烃类组成的混合物,为了简化其燃烧反应机理,诸多学者采用少数几种单一化学组分来表征其燃烧氧化特性和理化特征.目前公认的是以正庚烷和异辛烷(基础燃料(PRF))2种单一组分来表征不同辛烷值的汽油,并以此骨架机理演化而得到各种汽油表征物燃料反应机理,如甲苯参比燃料(TRF)机理、多组分混合物机理[2]等.
在乙醇的氧化机理研究方面,Marinov[3]提出了一种乙醇化学反应动力学机理并得到了学术界的一致认可,但该机理存在低温反应预测精度待提高以及与计算流体力学(CFD)多维模拟耦合计算耗时长等问题.此后其他学者以此为基础对乙醇的氧化机理进行了持续的改进和简化.
随着乙醇汽油的推广应用,混合燃料燃烧过程的准确模拟显得愈发重要,而目前关于乙醇汽油混合燃料的化学反应动力学机理的相关研究还较少,尤其是有关含水乙醇汽油燃烧机理鲜有报道.本文引入“半解耦”方法,以H2/CO/C1小分子机理为“内核”,耦合乙醇氧化骨架机理和汽油表征燃料的TRF机理,构建了一种四组分(异辛烷、正庚烷、甲苯和乙醇)燃料的乙醇汽油化学反应动力学模型.与相关文献实验结果进行多工况、宽范围的对比,结果表明该模型能够准确地模拟单组分和多组分燃料的着火延迟期和层流燃烧速度.进一步分析H2O的物质敏感性,在乙醇汽油机理的基础上调整添加H2O的反应,建立了含水乙醇汽油简化化学反应动力学模型,并与乙醇汽油着火特性实验数据对比,验证了该简化机理的合理性.
1 乙醇汽油简化化学反应动力学模型的构建 1.1 汽油和乙醇化学反应机理的研究现状国内外对汽油表征燃料反应机理进行了深入研究,建立了多种有关基础燃料燃烧的骨架机理模型、简化机理模型和详细机理模型.骨架机理模型属于经验模型,其中Shell模型由于简便实用而被广泛应用于发动机自燃着火的模拟研究,但其无法描述中间产物的变化和反映整个燃烧过程[4].Curran等[5]提出的PRF机理和Mehl等[6]提出的TRF机理是目前最详细的汽油表征燃料反应机理.详细机理模型的模拟效果及通用性较好,但过于复杂,计算量庞大.简化机理模型则能够在一定条件下模拟基础燃料的着火燃烧过程,虽然适用范围有限、精度相对较低,但是易于和CFD耦合计算.Liu等[7]构建了一个包含56种组分和168个反应的TRF简化机理,在多种反应器以及均质压燃(HCCI)发动机中不同工况下对该机理进行了实验验证,并将该机理应用于CONVERGE软件.
如前文所述,基于早期经典的Marinov[3]所提出的一种包含56种组分和372个基元反应的详细乙醇氧化机理,诸多学者进行了后续研究.Metcalfe等[8]发展了一种C1~C2小分子烃类和含氧燃料的详细机理,这些小分子燃料和中间体的反应特性对准确理解燃烧特性(着火延迟期、燃烧速度和排放物质等)至关重要.Mittal等[9]对Metcalfe等[8]的机理进行了改进,提出了一种包含111种组分、710个基元反应的乙醇燃烧详细机理.在环境压力p为1~5 MPa、温度T为825~985 K和当量比ϕ为0.3~1.0的条件下进行了着火延迟期的验证,该详细机理相较于Marinov机理对乙醇的低温反应模拟更加准确.
1.2 乙醇汽油简化化学反应动力学模型的构建为了准确反映乙醇汽油混合燃料的燃烧化学特性,并易于在CFD软件中进行数值模拟,需要建立混合燃料的化学反应动力学简化机理模型.考虑到汽油表征组分和乙醇氧化反应的温度特性,本文引入“半解耦”方法进行机理构建,即把燃料燃烧的高、低温区的机理分开考虑,低温区的反应由低温反应和“内核”(H2/CO/C1~Cn机理)一起控制,而高温区的反应仅受“内核”专门控制.利用小分子“内核”机理描述详细燃烧过程,骨架机理描述大分子氧化和大分子至小分子之间的过渡反应,在保证机理对燃烧特征参数准确预测的同时,又能简化机理规模.
通过乙醇反应路径分析和敏感性分析法,考虑“半解耦”方法对构建乙醇骨架机理的适用性,本文选用Mittal等[9]提出的乙醇详细机理.
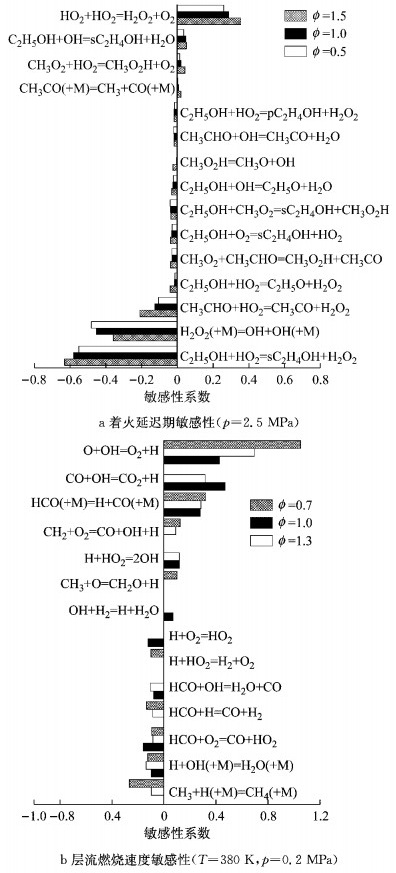
乙醇燃烧的反应过程分为反应链引发、活性基积累以及着火燃烧3个阶段.着火延迟期和层流燃烧速度分别反映了低温和高温反应特性.反应链引发和活性基积累阶段属于低温燃烧阶段,如图 1a所示.图 1中, M表示第三体, sC2H4OH和pC2H4OH为同分异构体.着火延迟期的敏感性分析结果显示,该阶段起主要作用的反应为O2、OH和HO2对乙醇的初始脱氢反应、CH3CHO的脱氢反应以及CH3CO的裂解反应.低温反应阶段的主要作用是通过放热提高整个系统的温度并产生大量的活性基群,为快速的高温反应提供温度环境和物质基础.层流燃烧速度敏感性分析(见图 1b)发现,敏感性系数高的反应均是C0~C1反应,这表明C0~C1反应控制着乙醇着火后的反应过程和火焰传播特性.HO2、OH、H2O2等在低温时生成,是自由基群开始的产物,同时参与乙醇、乙醛等的脱氢氧化,大大促进了高温反应,同时也是着火链分支的关键物质.HO2、OH等自由基在乙醇燃烧低温和高温反应之间的过渡中作用明显,将两者强烈地耦合在一起.因此,乙醇燃烧机理符合“半解耦”方法构建简化机理的思想.最后, 利用“半解耦”方法对Mittal等[9]提出的乙醇详细机理进行简化,得到了包含16种组分和26个基元反应的乙醇氧化骨架机理.
|
图 1 乙醇机理敏感性分析 Fig.1 Sensitivity analysis of ethanol mechanism |
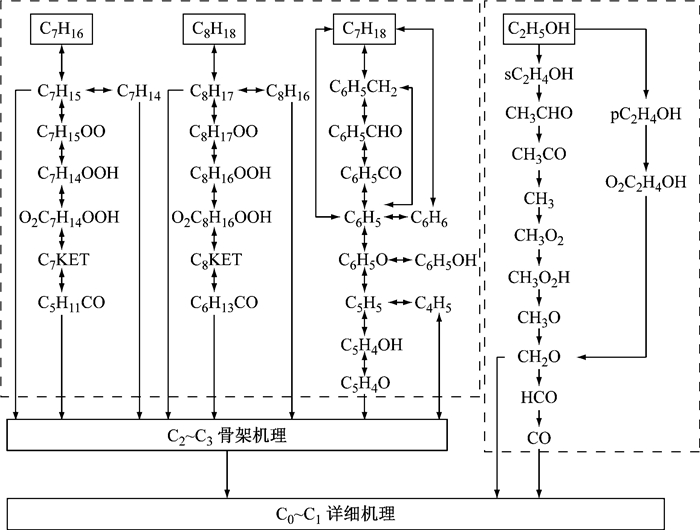
本文乙醇汽油简化机理的构建,以Klippenstein等[10]的H2/CO/C1小分子机理作为“内核”,将乙醇骨架机理耦合到Liu等[7]的TRF简化机理中,最终构建了乙醇汽油的简化化学反应动力学机理.由于乙醇含氧,其分子结构不同于烷烃和芳香烃,在进行机理构建时需要调整部分反应路径,将骨架机理与核心机理耦合起来,并删除重复组分和反应.耦合后的乙醇汽油简化机理的反应路径如图 2所示.图 2中, C7KET和C8KET表示过氧化氢酮.
|
图 2 乙醇汽油反应机理架构 Fig.2 Kinetic model sketch of ethanol-gasoline |
由于TRF机理和H2/CO/C1小分子机理都已经过广泛的实验验证,因此只针对乙醇汽油机理中乙醇骨架机理的动力学参数进行调整.分析参数的变化对着火延迟期敏感性的影响,寻找影响较大的基元反应,从而调整化学反应动力学参数,减小计算结果与实验数据的偏差[11].由Arrhenius方程分析可知,动力学模型的修正主要是对指前因子A进行适当调整.
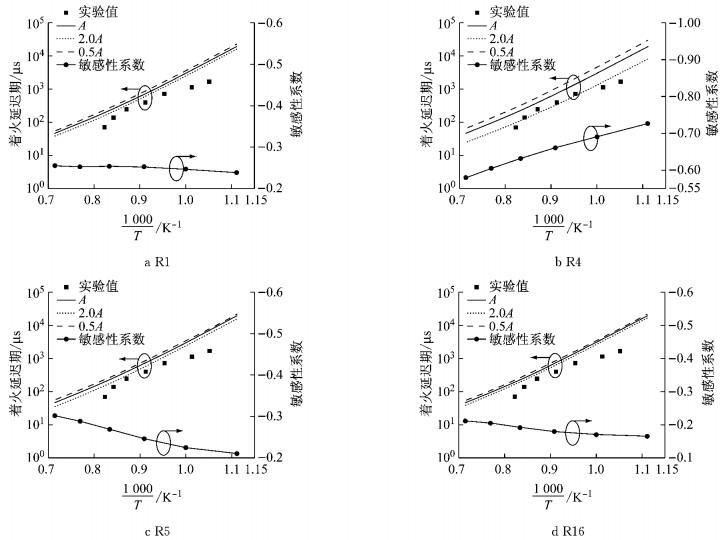
本文通过与Cancino等[12]的实验结果对比,同时分析不同温度下的敏感性系数,结果发现编号为R1、R4、R5和R16的反应对乙醇的着火延迟期有较大影响,分析结果如图 3所示.敏感性系数为负表示促进燃烧,反之阻碍燃烧,绝对值越大说明对燃烧的促进或抑制作用越强.4个反应的敏感性系数均小于零,说明均对乙醇燃烧起促进作用.编号为R1、R5和R16的反应敏感性系数绝对值随温度升高而增大,而编号为R4的反应敏感性系数绝对值则是随温度升高而减小.综合考虑敏感性分析结果中各基元反应的抑制和促进作用,反复调整各基元反应的指前因子,促使该乙醇汽油化学反应动力学模型的计算结果与实验数据更加吻合,最终得到的化学反应动力学因子修正结果如表 1所示.
|
图 3 R1、R4、R5和R16着火延迟期敏感性分析(ϕ=1.0, p=1 MPa) Fig.3 Sensitivity analysis of ignition delay time for R1, R4, R5 and R16(ϕ=1.0, p=1 MPa) |
| 下载CSV 表 1 乙醇骨架机理基元反应的动力学参数修正 Tab.1 Modification of kinetic parameters of ethanol skeleton mechanism |
燃料的着火延迟期是表征燃料着火和燃烧特性的一个重要参数,也是开发和验证燃烧化学反应动力学模型的一个重要参数.本文将OH浓度达到峰值的时刻定义为着火时刻,将化学反应开始到OH浓度达到峰值所经历的时间间隔作为着火延迟期.
层流燃烧速度指一维绝热平面的火焰面相对于来流未燃预混气体的速度,是任何可燃混合物的一个基本性质.由于预混层流燃烧的燃烧特性更加直接反映燃料的本质特性,因此在机理研究中将其作为一个重要验证指标.
球形膨胀火焰的前锋面是半径为r的球面,拉伸火焰传播速度Sn的计算公式如下所示[13]:
| $ {S_{\text{n}}} = \frac{{{\text{d}}r}}{{{\text{d}}t}} $ | (1) |
火焰前锋面的拉伸率
| $ \alpha = \frac{{d{A_{\text{f}}}}}{{{A_{\text{f}}}{\text{d}}t}} = \frac{2}{r}{S_{\text{n}}} $ | (2) |
式中:Af为火焰前锋面积.在火焰受点火影响之后,蜂窝化火焰形成之前,拉伸火焰传播速度与拉伸率α成线性关系,如下所示:
| $ {S_{\text{s}}} - {S_{\text{n}}} = {L_{\text{b}}}\alpha $ | (3) |
式中:Lb为Markstein长度;Ss为无拉伸火焰传播速度,当α=0时,Ss=Sn.由火焰前锋面的质量守恒可得层流燃烧速度
| $ {S_{\text{L}}} = \frac{{{\rho _{\text{b}}}}}{{{\rho _{\text{u}}}}}{S_{\text{s}}} = \frac{{{\rho _{\text{b}}}}}{{{\rho _{\text{u}}}}}\left( {1 + {L_{\text{b}}}\frac{2}{r}} \right)\frac{{{\text{d}}r}}{{{\text{d}}t}} $ | (4) |
式中:ρb是化学平衡状态下燃烧混合物的密度;ρu是初始条件下未燃混合物的密度, 在绝热火焰温度下计算得到.由于乙醇汽油化学反应动力学机理由正庚烷、异辛烷、甲苯和乙醇4种组分构成,在燃烧过程中各个组分会彼此产生干扰,因此需要对单组分和多组分都进行计算值与实验值的对比验证.
2.1 着火延迟期的验证在CHEMKIN软件中采用零维绝热模型,在定容和均质条件下计算着火延迟期.
在不同压力和当量比条件下计算了TRF机理中单组份和多组分物质的着火延迟期,并与相应的实验结果进行对比,取得了较好的一致性.本文重点对乙醇及乙醇汽油的着火延迟期进行验证对比.
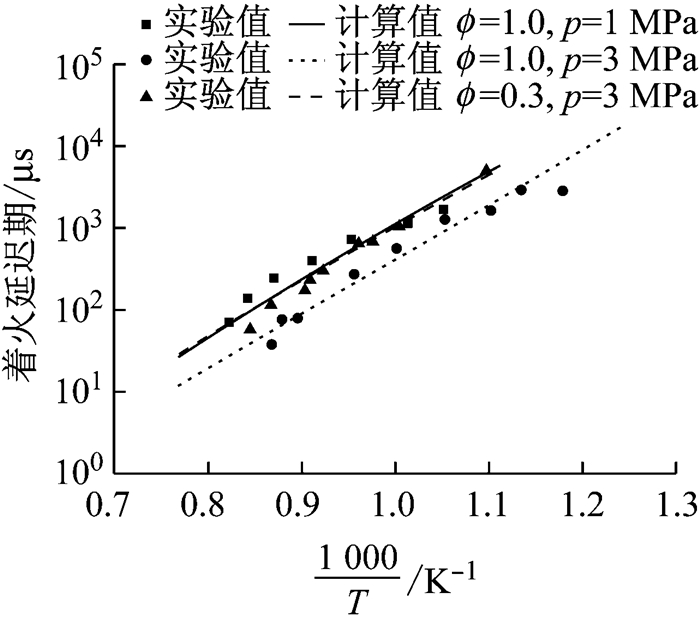
图 4展示了乙醇着火延迟期的验证结果,实验数据取自Cancino等[12]的研究成果.由图 4可知,乙醇着火延迟期的计算值与实验值较为吻合,体现了随温度变化的趋势,没有负温度效应(即随着温度的增加,总体反应率不增反降).同时,在稀混合气条件下(ϕ=0.3)着火延迟期明显增大.
|
图 4 乙醇着火延迟期计算值与实验值的对比 Fig.4 Comparison of ignition delay time of ethanol between calculation results and experimental results |
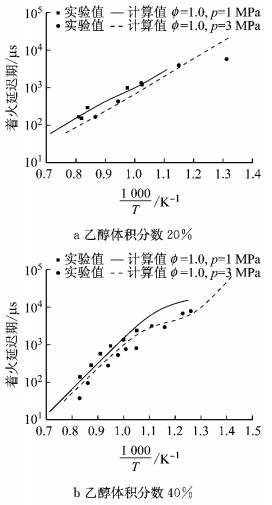
图 5所示为不同压力和乙醇体积分数下乙醇汽油混合燃料着火延迟期的验证结果,其中实验数据分别取自Fikri等[14]和Cancino等[15]的研究成果.由图 5可知,乙醇汽油着火延迟期的计算值与实验值随温度变化的趋势基本保持一致.乙醇体积分数为40%时的偏差较20%时的更为明显,并且由于实验值较少,在个别点偏差较为显著.
|
图 5 乙醇汽油着火延迟期计算值与实验值的对比 Fig.5 Comparison of ignition delay time of ethanol-gasoline between calculation results and experimental results |
综合本文乙醇汽油简化化学反应动力学模型中单组分和多组分着火延迟期的验证结果可知,本文机理的计算值与实验值基本保持一致,能够准确反映着火延迟期随温度变化的关系.此外,着火延迟期随当量比和压力的升高而降低,并且甲苯和乙醇都没有出现负温度效应,这也体现了乙醇汽油燃烧过程的低温反应特性.由于低温实验点较少,计算结果仅反映了趋势,实验研究有待进一步发展.
2.2 层流燃烧速度的验证本文采用CHEMKIN软件中的预混火焰模型计算单组分及多组分燃料的层流燃烧速度.
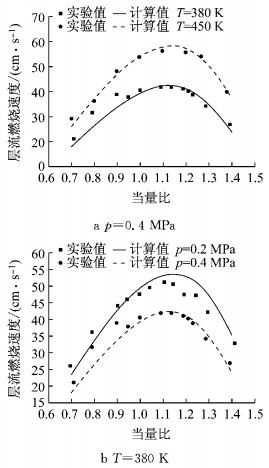
不同温度和压力条件下TRF机理单组分与多组分物质的层流燃烧速度的计算值与实验值基本一致.图 6展示了乙醇层流燃烧速度与当量比的关系,实验数据取自Nathan[16]的研究结果.由图 6可知,除了在0.2 MPa、380 K条件下计算值与实验值偏差稍大,其余条件下乙醇层流燃烧速度的计算值与实验值基本吻合,并且在当量比大于1.0的条件下计算结果的准确性更高.
|
图 6 乙醇层流燃烧速度计算值与实验值的对比 Fig.6 Comparison of laminar burning velocity of ethanol between calculation results and experimental results |
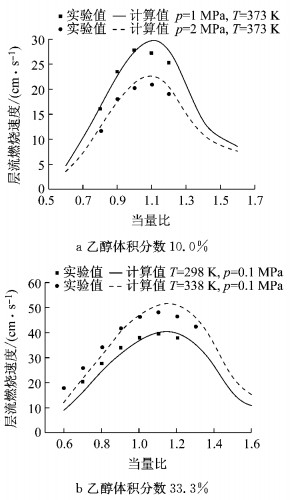
图 7展示了在不同乙醇体积分数下乙醇汽油层流燃烧速度的验证结果.实验数据分别取自Lipzig等[17]、Dirrenberger等[18]和Jerzembeck等[19]的研究成果.从图 7可以看出,在当量比小于1.2的条件下,乙醇汽油层流燃烧速度的计算值与实验值有较好的一致性,在当量比大于1.2的条件下由于实验数据较少,两者对比偏差较大,但仍能看出该模型基本模拟出乙醇汽油层流燃烧速度随当量比升高的变化趋势.
|
图 7 乙醇汽油层流燃烧速度计算值与实验值的对比 Fig.7 Comparison of laminar burning velocity of ethanol-gasoline between calculation results and experimental results |
综合本文乙醇汽油简化化学反应动力学模型中单组分和多组分层流燃烧速度的验证结果可知,计算值与实验值基本保持一致,本文机理能够准确预测出燃烧过程层流燃烧速度随当量比升高而先升后降的变化关系,反映出乙醇汽油燃烧过程的高温反应特性,当乙醇含量较高时,模拟结果更为准确.此外,初始反应温度的升高能提高层流燃烧速度,而压力升高则使层流燃烧速度下降,这也从侧面体现了本文机理模拟的准确性.
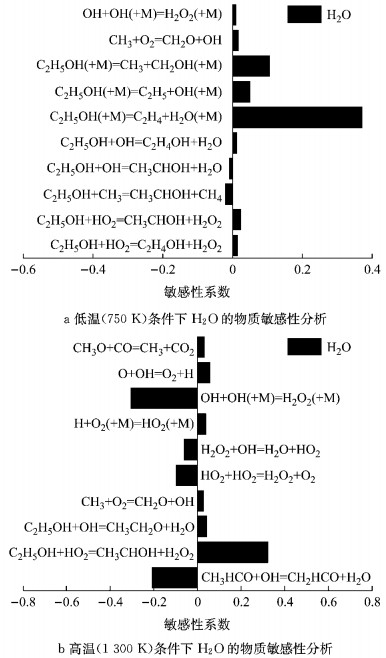
3 含水乙醇汽油简化化学反应动力学模型的构建与验证为了研究含水乙醇中水的化学作用对含水乙醇汽油燃烧过程的影响,对高、低温反应阶段H2O的物质敏感性进行分析,找出促进和抑制H2O物质生成的重要基元反应,如图 8所示.由图 8可看出,在低温反应阶段乙醇的裂解以及高温反应阶段被HO2氧化的反应对H2O生成的促进作用明显,而在高温阶段OH的自身消耗反应对H2O生成的抑制作用比较明显.中间自由基CH3的氧化反应无论是在高温还是在低温反应阶段,都对促进H2O的生成起重要作用[20].
|
图 8 高、低温反应阶段H2O的物质敏感性分析 Fig.8 Sensitivity analysis of H2O at high and low temperature reactions |
此外,在H2O的物质敏感性分析结果中发现,OH、H自由基反应对H2O具有敏感性,因此在基元反应O+OH=O2+H、H+O2(+M)=HO2(+M)和OH+OH=O+H2O的基础上,再增加与H2O物质生成相关的重要基元反应,具体如下所示:
H+H(+M)=H2(+M)
O+H2=H+OH
H+OH(+M)=H2O(+M)
HO2+H=H2+O2
HO2+O=OH+O2
将上述与H2O生成相关的重要基元反应与乙醇汽油燃烧简化机理耦合在一起,建立了包含65种物质、194个基元反应的含水乙醇汽油的简化化学反应动力学模型.
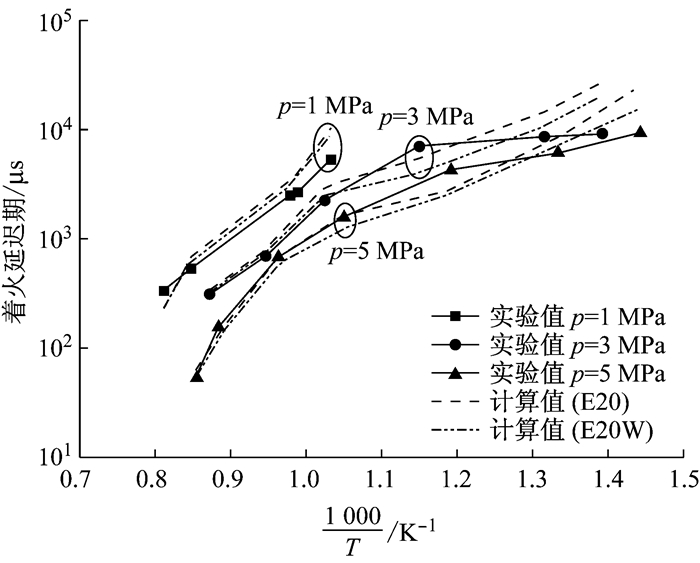
由于目前关于含水乙醇汽油燃烧化学动力学机理的研究较少,检索不到有关其着火特性的相关实验数据,因而只能对含水乙醇汽油的着火延迟期计算值与乙醇汽油着火延迟期的实验值进行比较,以验证含水乙醇汽油燃烧简化动力学模型的趋势准确性.图 9给出了在当量比ϕ为1.0,初始压力p分别为1 MPa、3 MPa和5 MPa条件下,含水乙醇汽油(E20W)和乙醇汽油(E20)的着火延迟期随初始温度的变化情况.在高温反应阶段,含水乙醇汽油着火延迟期的计算值与乙醇汽油实验值吻合较好,除了个别点外最大偏差不超过20%.在低温反应阶段,含水乙醇着火延迟期的模拟结果与实验结果存在一定偏差,但曲线发展趋势大致相同.总之,含水乙醇汽油着火延迟期的计算值与乙醇汽油的实验值趋势基本一致,能够体现出含水乙醇汽油的燃烧化学特性.
|
图 9 含水乙醇汽油着火延迟期计算值与乙醇汽油着火延迟期实验值的对比(ϕ=1.0) Fig.9 Comparison of ignition delay time between calculation results of hydrous ethanol-gasoline and experimental results of ethanol-gasoline(ϕ=1.0) |
本文引入“半解耦”方法并进行乙醇详细机理简化的适用性分析,得到了乙醇氧化骨架机理.进一步与汽油TRF机理和H2/CO/C1小分子机理耦合,构建了包含4个组分(异辛烷、正庚烷、甲苯、乙醇)的乙醇汽油反应机理,并利用敏感性分析法修正了部分基元反应的动力学参数.
利用本文构建的乙醇汽油简化化学反应动力学模型进行仿真计算并与实验值对比,结果表明本文模型可以准确模拟单组分和多组分燃料的着火延迟期与层流燃烧速度,并反映出燃烧特性随当量比、温度与压力变化的趋势,从而验证了乙醇汽油机理的合理性与准确性.
通过对H2O的物质敏感性分析,在乙醇汽油机理的基础上添加有关H2O的反应机理,构建了包含65种物质和194个基元反应的含水乙醇汽油简化化学反应动力学模型.通过与乙醇汽油着火延迟期的实验结果进行比较,验证了含水乙醇汽油简化机理的合理性.
| [1] |
陈振斌, 倪计民, 张惜辉, 等. 乙醇-丁醇-柴油混合燃料的车辆排放性和经济性[J]. 农业工程学报, 2012, 28(7): 62 CHEN Zhenbin, NI Jimin, ZHANG Xihui, et al. Vehicle emission and fuel consumption of diesel vehicles fueled with ethanol-butanol-diesel blends[J]. Transactions of the Chinese Society of Agricultural Engineering, 2012, 28(7): 62 DOI:10.3969/j.issn.1002-6819.2012.07.011 |
| [2] |
刘耀东.基础燃料(PRF)及汽油表征燃料(TRF)化学反应动力学骨架模型的研究[D].大连: 大连理工大学, 2013. LIU Yaodong. Research on the development of skeletal chemical kinetic models for primary reference fuel and gasoline surrogate fuel(TRF)[D]. Dalian: Dalian University of Technology, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10141-1013197993.htm |
| [3] |
MARINOV N M. A detailed chemical kinetic model for high temperature ethanol oxidation[J]. International Journal of Chemical Kinetics, 1999, 31(3): 183 DOI:10.1002/(ISSN)1097-4601 |
| [4] |
ZHEN X, WANG Y, LIU D. An overview of the chemical reaction mechanisms for gasoline surrogate fuels[J]. Applied Thermal Engineering, 2017, 124: 1257 DOI:10.1016/j.applthermaleng.2017.06.101 |
| [5] |
CURRAN H J, PITZ W J, WESTBROOK C K, et al. Oxidation of automotive primary reference fuels at elevated pressures[J]. Symposium on Combustion, 1998, 27(1): 379 DOI:10.1016/S0082-0784(98)80426-8 |
| [6] |
MEHL M, PITZ W J, WESTBROOK C K, et al. Kinetic modeling of gasoline surrogate components and mixtures under engine conditions[J]. Proceedings of the Combustion Institute, 2011, 33(1): 193 DOI:10.1016/j.proci.2010.05.027 |
| [7] |
LIU Y D, JIA M, XIE M Z, et al. Development of a new skeletal chemical kinetic model of toluene reference fuel with application to gasoline surrogate fuels for computational fluid dynamics engine simulation[J]. Energy & Fuels, 2013, 27(8): 4899 |
| [8] |
METCALFE W K, BURKE S M, AHMED S S, et al. A hierarchical and comparative kinetic modeling study of C1-C2, hydrocarbon and oxygenated fuels[J]. International Journal of Chemical Kinetics, 2013, 45(10): 638 DOI:10.1002/kin.2013.45.issue-10 |
| [9] |
MITTAL G, BURKE S M, DAVIES V A, et al. Autoignition of ethanol in a rapid compression machine[J]. Combustion & Flame, 2014, 161(5): 1164 |
| [10] |
KLIPPENSTEIN S J, HARDING L B, DAVIS M J, et al. Uncertainty driven theoretical kinetics studies for CH3OH ignition: HO2+CH3OH and O2+CH3OH[J]. Proceedings of the Combustion Institute, 2011, 33(1): 351 DOI:10.1016/j.proci.2010.05.066 |
| [11] |
苏万华, 赵华, 王建昕, 等. 均质压燃低温燃烧发动机理论与技术[M]. 北京: 科学出版社, 2010 SU Wanhua, ZHAO Hua, WANG Jianxin, et al. Engine theory and technology of homogeneous charge compression combustion and low temperature combustion[M]. Beijing: Science Press, 2010 |
| [12] |
CANCINO L R, FIKRI M, OLIVEIRA A A M, et al. Measurement and chemical kinetics modeling of shock-induced ignition of ethanol-air mixtures[J]. Energy & Fuels, 2010, 24(5): 2830 |
| [13] |
BRADLEY D, HICKS R A, LAWES M, et al. The measurement of laminar burning velocities and Markstein numbers for iso-octane-air and iso-octane-n-heptane-air mixtures at elevated temperatures and pressures in an explosion bomb[J]. Combustion & Flame, 1998, 115(1/2): 126 |
| [14] |
FIKRI M, HERZLER J, STARKE R, et al. Autoignition of gasoline surrogates mixtures at intermediate temperatures and high pressures[J]. Combustion & Flame, 2008, 152(1): 276 |
| [15] |
CANCINO L R, FIKRI M, OLIVEIRA A A M, et al. Ignition delay times of ethanol-containing multi-component gasoline surrogates: shock-tube experiments and detailed modeling[J]. Fuel, 2011, 90(3): 1238 DOI:10.1016/j.fuel.2010.11.003 |
| [16] |
NATHAN I D H. Measuring laminar burning velocities using constant volume combustion vessel techniques[D]. Oxford: University of Oxford, 2014.
|
| [17] |
LIPZIG J P, NILSSON E J K, GOEY L. Laminar burning velocities of n-heptane, iso-octane, ethanol and their binary and tertiary mixtures[J]. Fuel, 2011, 90: 2773 DOI:10.1016/j.fuel.2011.04.029 |
| [18] |
DIRRENBERGER P, GLAUDE P A, BOUNACEUR R, et al. Laminar burning velocity of gasolines with addition of ethanol[J]. Fuel, 2014, 115(1): 162 |
| [19] |
JERZEMBECK S, GLAWE C, PETERS N. Development and experimental evaluation of a high temperature mechanism for blended n-heptane-isooctane-ethanol-air-mixtures and gasoline-ethanol-air-mixtures[C]//World Scientific and Engineering Academy and Society (WSEAS) Stevens Point. Wisconsin: [s.n.], 2009: 79-83.
|
| [20] |
LIANG J, LI G, ZHANG Z, et al. Experimental and numerical studies on laminar premixed flames of ethanol-water-air mixtures[J]. Energy & Fuels, 2014, 28(7): 4754 |
 2018, Vol. 46
2018, Vol. 46
